FDA pina-recall ang chemo drug na kontaminado ng ‘bacteria’
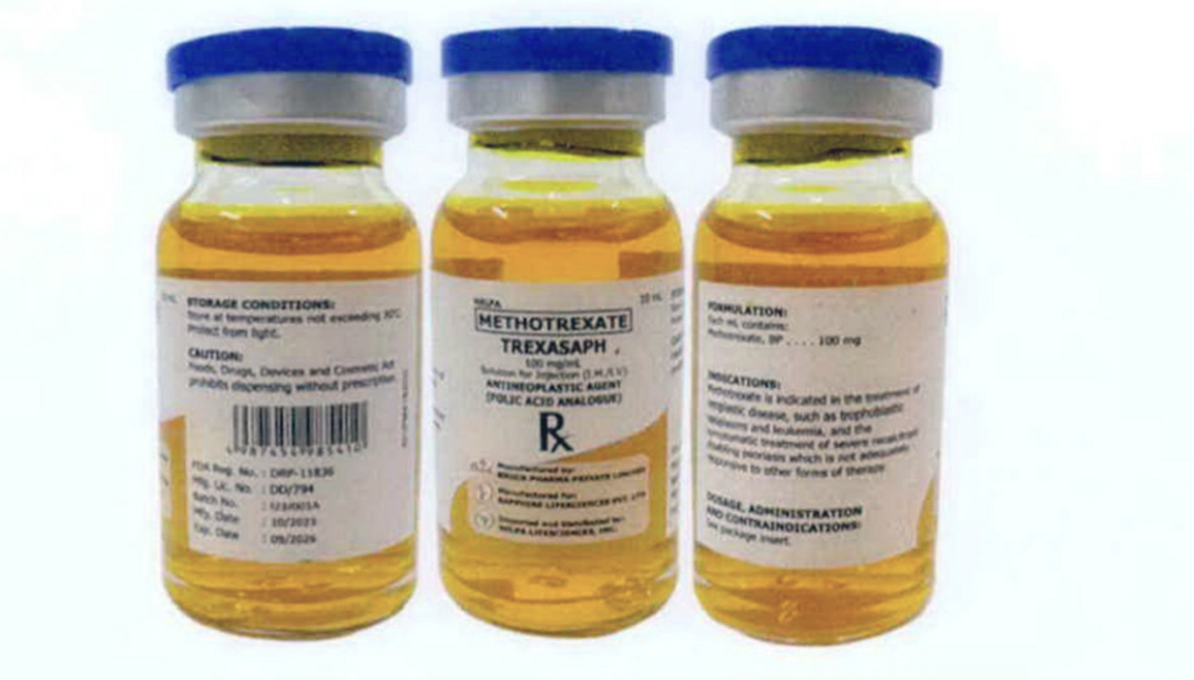
INQUIRER file photo
NAGLABAS na ng pangalawang kautusan ang Philippine Food and Drug Administration (FDA) kaugnay sa pag-recall ng imported na chemotherapy drug na “Trexasaph.”
Ito ay matapos malaman na karamihan nito ay kontaminado sa bacteria na nagdudulot ng nakamamatay na impeksyon.
Sa ilalim ng Advisory No. 2024-0741 ng ahensya na may petsang May 3, iniutos ni FDA Director General Dr. Samuel Zacate ang product recall o pagbabalik ng Trexasaph (na may generic na pangalan na Methotrexate) 100 mg/mL solution for injection (IM/IV) na may Batch Numbers na I23F025A, I23J001A, I23K002A at I23H018A.
Para sa kaalaman ng marami, ang Methotrexate ay isang chemotherapy agent at immune system suppressant.
Ginagamit ito bilang treatment sa neoplastics disease (cancers), katulad ng trophoblastic neoplasms at leukemia, pati na rin sa symptomatic treatment ng psoriasis na hindi tumutugon sa iba pang mga paraan ng therapy.
Baka Bet Mo: FDA sa publiko: I-report ang mga nararanasang ‘side effects’ sa mga gamot
Ang mga gumagamit nito ay may side effects na maaaring humina ang immune system at mas maging vulnerable sa mga impeksyon.
“Following the received adverse reaction report involving a pediatric patient administered with Trexasaph, the [FDA] conducted laboratory analysis on the collected samples. The Trexasaph with Batch No. I23J001A failed the sterility test and was found positive with Pseudomonas aeruginosa, indicating contamination of the products,” sey ng FDA.
Ang Pseudomonas aeruginosa ay karaniwang nakukuha ng mga pasyente na naco-confine sa ospital ng mahigit isang linggo.
Maaari itong maging sanhi ng impeksyon sa daloy ng dugo o sepsis na maaaring humantong sa kamatayan.
Anumang produkto na may anumang kontaminasyon at direktang ibinibigay sa katawan ay magpapakita ng malubhang panganib sa mga pasyente.
Maaaring lumaki at kumalat ang bacteria sa maraming iba’t ibang paraan, kabilang ang sa pamamagitan ng tubig (mula sa mga lababo, bathtub, pool, hot tub, humidifier, at kusina), lupa, pagkain, at kontaminadong mga medikal na kagamitan (tulad ng mga ventilator o urinary catheter).
Ang impeksyon ng Pseudomonas aeruginosa ay maaari ring dumaan from person to person –kadalasan mula sa kontaminadong kamay.
Dahil sa seryosong impeksyon, iniutos na ng FDA sa mga ospital, retailers, distributors, pharmacies at clinics na itigil na ang pag-distribute, pagbenta at paggamit ng Trexasaph.
Pinaalalahanan din ang consumers na huwag gamitin o bumili ang nasabing produkto.
“All local government units and law enforcement agencies are requested to ensure that the affected product lot is not sold or made available in their localities or areas of jurisdiction,” lahad ng ahensya.
Batay sa database ng FDA, ang nasabing gamot ay ginawa ng Bruck Pharma Private Ltd. na nakabase sa India at ini-import ng Nelpa Lifesciences Inc. sa Parañaque City.
Ito ay nakarehistro sa FDA mula May 2022 at ang pagpaparehistro nito ay nakatakdang mag-expire sa Mayo 2027.
Noong Marso nang unang pina-recall ang nabanggit na gamot matapos magpositibo sa Pseudomonas aeruginosa ang Batch No. I23J001A.
Upang i-report ang patuloy na pagbenta at distribution ng affected batches ng Trexasaph, pwedeng magpadala ng email sa FDA via [email protected] o kaya tumawag sa Center for Drug Regulation and Research sa numerong (02) 8809-5596.
Disclaimer: The comments uploaded on this site do not necessarily represent or reflect the views of management and owner of Bandera. We reserve the right to exclude comments that we deem to be inconsistent with our editorial standards.




